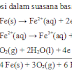PEMBUATAN
TAWAS ALUMUNIUM
I.
TUJUAN
-Untuk mengetahui proses pembuatan
tawas aluminium dalam laboratorium.
-Untuk mengetahui proses sintesis
tawas aluminium dalam industri.
-Untuk mengetahui manfaat dari
penggunaan tawas aluminium.
II.
DASAR TEORI
Lingkungan hidup adalah semua benda yang hidup
(biotik) dan yang tidak hidup (abiotik) serta kondisi yang ada dalam ruang yang
kita tempati. Antara manusia dan lingkungan terdapat hu ungan timbal balik,
manusia mempengaruhi lingkungannya begitu juga sebaliknya. Jika lingkungan
tercemar maka manusia akan merasakan dampaknya. Persoalan lingkungan yang ada
hampir selalu ditimbulkan oleh ulah manusia dan kegiatan produksi yang
dilakukannya. Kedua aktivitas ini merupakan sumber pencemaran lingkungan karena
menggunakan dan menghasilkan zat atau bahan yang berbahaya yang tidak dapat di
daur ulang (Nurhasmawaty, 2004).
Kegiatan produksi selain menghasilkan produk yang
mempunyai nilai ekonomi juga menghasilkan limbah, berupa limbah padat, cair
maupun gas. Limbah-limbah tersebut akan menyebabkan pencemaran lingkungan
meliputi pencemaran air, pencemaran udara, dan pencemaran tanah.
Pencemaran tanah dapat terjadi akibat penggunaan
pupuk secara berlebihan, penggunaan pestisida dan pembuangan limbah yang tidak
dapat terurai. Saat ini banyak dijumpai limbah yang tidak dapat diurai seperti
plastik, karet, kaleng, dan botol, karena manusia cenderung menginginkan
kemudahan dan keindahan dalam hidupnya. Botol minuman dibuat dari kaleng dan
plastik agar ringan dan tidak pecah bila terjatuh. Menjinjing makanan lebih
menarik dan bersih dengan kantong plastik daripada dibungkus dengan daun pisang
atau daun jati. Penggantian bahan-bahan tersebut dari segi ekonomi lebih
menguntungkan tetapi jika dilihat dari dampak lingkungan hal tersebut merugikan
karena akan menambah jumlah limbah yang tidak dapat diurai. Akibatnya
pencemaran lingkungan semakin bertambah (Tejoyuwono, 2006).
Limbah merupakan konsekuensi dari adanya aktifitas
manusia karena setiap aktifitas manusia cenderung menghasilkan limbah atau
buangan. Jumlah/volume sampah sebanding dengan tingkat konsumsi manusia
terhadap
barang/material
yang digunakan sehari-hari. Salah satu limbah yang banyak ditemukan di
lingkungan adalah limbah kaleng. Jika disebutkan satu per satu banyak sekali
limbah kaleng yang dihasilkan oleh manusia dalam kehidupan sehari-hari. Proses
daur ulang akan menghemat energi dan eksploitasi sumber daya alam sekaligus
mengurangi timbunan sampah di TPA (Pahlano, 2007).
Selain untuk mengurangi pencemaran lingkungan dan
timbunan sampah di TPA, proses daur ulang juga dapat menambah nilai ekonomis
dari limbah kaleng terutama recovery dari logam-logam seperti aluminium,
seng, timah, atau besi. Dugaan kuat bahwa beberapa kaleng bekas mengandung
aluminium dengan kadar yang bervariasi, mengingat aluminium mempunyai sifat
tahan korosi, ringan dan mudah di dapat sehingga memungkinkan untuk dijadikan
bahan baku kaleng. Kandungan aluminium dalam kaleng bekas juga memberi peluang
untuk diolah menjadi bahan koagulan penjernih air (tawas) atau bahan dalam deodorant.
Daya koagulasi tawas yang di dapat akan di bandingkan dengan tawas dari pasaran
dengan metode turbidimetri. Mengingat banyaknya minuman ringan yang diproduksi
dan menggunakan kemasan kaleng serta dampak yang ditimbulkan terhadap
lingkungan, maka diperlukan penelitian terhadap kandungan aluminium dari
beberapa jenis kaleng minuman ringan. Kaleng bekas minuman ringan yang
mengandung aluminium selanjutnya diolah menjadi bahan koagulan penjernih air
(tawas).
III. ALAT DAN BAHAN
Alat:
-Erlenmeyer
-Gelas
beaker
-Gelas
Ukur
-Gunting
-Amplas
-Batang
Pengaduk
-Corong
-Turbidimeter varian DMS 80 UV visible
spektrofotometer dan spektrofometer serapan atom AA-6200
Bahan:
-KOH 20%
-Accu Zur
-Etanol 50%
-AlCl3
-Aquadest
-NaOH 10%
-Soda Api 25%
-3 Kaleng bekas
IV. Cara Kerja
V.
HASIL PENGAMATAN
No.
|
Kaleng Bekas
|
Ditambahkan
|
Hasil
|
Berat Tawas
|
Berat Kertas Saring (gr)
|
1
|
A
|
50 ml KOH 20%
|
Terbentuk Tawas
|
6,34
|
1,65
|
2
|
B
|
50 ml soda api 25%
|
Tidak terbentuk tawas
|
-
|
-
|
3
|
C
|
50 ml NaOH 10%
|
Tidak terbentuk tawas
|
-
|
-
|
VI.
REAKSI DAN PERHITUNGAN
2Al
+ 2KOH + 6H2O -------> 2K[Al(OH)4] +
3H2
2K[Al(OH)4]+H2SO4 -------> Al(OH)3+K2SO4+2H2O
2Al(OH)3 + 3H2SO4 -------> Al2(SO4)3 + 6H2O
K2SO4+Al2(SO4)3+12H2O------->2KAl(SO4)2.12H2O
Diketahui
: Berat Kertas Saring : 1,65 dimisalkan
a
Berat Kertas Saring+Tawas : 7,99 dimisalkan b
Ditanya : Berat Tawas?
Penyelesaian:
Berat Tawas = a-b
=
7,99 – 1,65 = 63,4 g
VII.
Pembahasan
Praktikum kali ini
adalah pembuatan tawas menggunakan bahan alumunium. Alumunium didapat dari
kaleng-kaleng bekas minuman. Untuk membedakan kaleng-kaleng tersebut diberi
nama A,B, dan C. Pembuatan tawas kali
ini dibagi menggunakan 3 cara. Cara pertama yaitu penambahan KOH 20% sebanyak
50 ml kedalam erlenmeyer yag telah berisi potongan-potogan kaleng/alumunium A. Pada penambahan KOH 20% reaksi berjalan cepat
dan bersifat eksoterm karena menghasilkan kalor. Reaksi yang terjadi adalah :
2Al + 2KOH + 6H2O ------->2K[Al(OH)4] +
3H2
Dalam reaksi ini terbentuk gas H2
yang ditandai dengan munculnya gelembung gelembung gas. Gelembung-gelembung gas
hilang setelah semua aluminium bereaksi. Untuk menghindari terbentuknya Al(OH)3 maka KOH 20% ditambahkan berlebih. Pada tahap
ini, dilakukan pemanasan untuk mempercepat reaksi. Filtrat yang diperoleh
ditambah H2SO4 6 M kemudian disaring untuk menghilangkan
pengotor-pengotornya. Reaksi yang terjadi adalah :
2K[Al(OH)4]+H2SO4------->2Al(OH)3+K2SO4+2H2O
Penambahan larutan H2SO4 dilakukan agar seluruh senyawa K[Al(OH)4] dapat bereaksi sempurna. Al(OH)3 yang terbentuk langsung bereaksi dengan H2SO4
dengan persamaan reaksi sebagai berikut :
2Al(OH)3 + 3H2SO4------->Al2(SO4)3 + 6H2O
Pada
reaksi sebelumnya, penambahan H2SO4 membentuk Al(OH)3 bersama-sama dengan K[Al(OH)4], namun setelah berlebih H2SO4
melarutkan Al(OH)3 menjadi
Al2(SO4)3 berupa larutan bening tak berwarna. Senyawa
Al2(SO4)3 yang terbentuk pada reaksi (3) di atas
bereaksi kembali dengan K2SO4 hasil reaksi (2) membentuk kristal yang
diperkirakan adalah KAl(SO4)2.12H2O
berwarna putih (anonim, 2006). Reaksinya adalah :
K2SO4+Al2(SO4)3+12H2O------->2KAl(SO4)2.12H2O
Kristal alum (tawas) yang diperoleh
dicuci dengan larutan etanol 50% yang bertujuan untuk menyerap kelebihan air
dan mempercepat pengeringan. Berat tawas yang diperoleh 6,34 gram . Makin besar kandungan aluminiumnya, makin
banyak tawas yang terbentuk.
Kemudian cara kedua yaitu dengan menambahkan
larutan soda api 25% sebanyak 25 ml ke bahan kaleng alumunium B. Pada percobaan
ini tidak terbentuk tawas, mungkin dapat diakibatkan karena larutan tidak
benar-benar larutan murni atau disebabkan juga oleh kesalahan praktikan saat
melakukan percobaan.
Terakhir pada cara ketiga yaitu
penambahan NaOH 10%. Sama halnya pada penambahan soda api 25% ,
penambahan NaOH 10% tidak menghasilkan terbentuknya tawas. Hal ini dapat
disebabkan oleh faktor-faktor yang sama pula.
Tawas yang dihasilkan nantinya dapat
digunakan dalam kehidupan sehari-hari contohnya untuk mengurangi kekeruhan pada
air.
VIII. KESIMPULAN
1. Berat
Tawas yang dihasilkan sebesar 6,34 g
2. Larutan
KOH 20% lebih efektif digunakan untuk menghasilkan tawas
3. Tawas
dapat digunakan untuk menjernihkan air
IX. DAFTAR PUSTAKA
http://ejournal.unud.ac.id/abstrak/j-kim-4-2-10.pdf
diakses pada tanggal 28 Oktober 2012
Cotton dan Wilkinson., 1989, Kimia
Anorganik Dasar, Penerbit UI Press, Jakarta, h. 287-288
Achmad, H., 1992, Kimia Unsur dan
Radio Kimia, Penerbit PT Citra Aditya Bakti, Bandung, 85-87